अध्याय 03 जैवअणु
पिछले अध्याय में आपने कोशिका और उसकी कोशिकांगों (organelles) के बारे में पढ़ा। प्रत्येक कोशिकांग की अलग संरचना होती है, इसलिए वे भिन्न-भिन्न कार्य करते हैं। उदाहरण के लिए, कोशिका झिल्ली लिपिड और प्रोटीन से बनी होती है; कोशिका भित्ती कार्बोहाइड्रेट से बनी होती है; गुणसूत्र (क्रोमोसोम) प्रोटीन और न्यूक्लिक अम्ल (DNA) से बने होते हैं; और राइबोसोम प्रोटीन तथा न्यूक्लिक अम्ल (RNA) से बने होते हैं। इन कोशिकांगों के ये घटक बृहत् अणु (macromolecules) या जैव अणु (biomolecules) कहलाते हैं। जैव अणु मुख्यतः चार प्रकार के होते हैं—कार्बोहाइड्रेट, प्रोटीन, लिपिड और न्यूक्लिक अम्ल। कोशिका की संरचना का हिस्सा होने के अतिरिक्त ये जैव अणु कोशिकीय क्रियाओं में महत्वपूर्ण भूमिका निभाते हैं। इस अध्याय में आप इन जैव अणुओं की संरचना और कार्यों का अध्ययन करेंगे।
3.1 कार्बोहाइड्रेट
कार्बोहाइड्रेट्स प्रकृति में जैव-अणुओं के सबसे प्रचुर वर्गों में से एक हैं और सभी जीवन-रूपों में व्यापक रूप से पाए जाते हैं। रासायनिक रूप से, ये बहु-हाइड्रॉक्सिल एल्कोहॉलों के ऐल्डिहाइड और कीटोन व्युत्पन्न होते हैं। जीवित जीवों में कार्बोहाइड्रेट्स की प्रमुख भूमिका प्राथमिक ऊर्जा स्रोत के रूप में कार्य करना है। ये अणु ऊर्जा भंडार, चयापचय मध्यवर्ती, और जीवाणुओं और पादप कोशिका भित्ति के प्रमुख घटकों में से एक के रूप में भी कार्य करते हैं। साथ ही, ये DNA और RNA का भी हिस्सा हैं, जिन्हें आप इस अध्याय में आगे पढ़ेंगे। जीवाणुओं और पादपों की कोशिका भित्तियाँ कार्बोहाइड्रेट्स के बहुलक से बनी होती हैं। कार्बोहाइड्रेट्स सूचनात्मक सामग्री के रूप में भी कार्य करते हैं और प्रोटीन और लिपिड की सतहों से जुड़कर कोशिका-कोशिका अन्योन्यक्रिया में, और कोशिकाओं के कोशिकीय वातावरण के अन्य तत्वों के साथ अन्योन्यक्रिया में भूमिका निभाते हैं।
(A) कार्बोहाइड्रेट्स का वर्गीकरण
कार्बोहाइड्रेट्स विभिन्न रूपों में पाए जाते हैं, सरल शर्कराओं से लेकर एक से अधिक इकाइयों के जटिल बहुलकों तक, और तदनुसार इन्हें वर्गीकृत किया गया है। इन्हें सामान्यतः तीन श्रेणियों में बाँटा गया है—मोनोसैकेराइड्स, ओलिगोसैकेराइड्स और पॉलिसैकेराइड्स।
1. मोनोसैकेराइड्स
मोनोसैकेराइड सरल शर्कराएँ होती हैं जिन्हें आगे सरल रूपों में हाइड्रोलाइज़ नहीं किया जा सकता। ये मोनोसैकेराइड सरबतम कार्बोहाइड्रेट होते हैं, जिनमें मुक्त ऐल्डिहाइड $(-\mathrm{CHO})$ और कीटोन $(>\mathrm{C}=\mathrm{O})$ समूह होते हैं, दो या अधिक हाइड्रॉक्सिल $(-\mathrm{OH})$ समूहों के साथ तथा सामान्य सूत्र $\mathrm{C} _n\left(\mathrm{H} _2 \mathrm{O}\right)_n$ होता है। कार्बन परमाणुओं की संख्या और क्रियात्मक समूहों के आधार पर, मोनोसैकेराइड्स को तालिका 3.1 में दिए गए अनुसार वर्गीकृत किया गया है।
तालिका 3.1: मोनोसैकेराइड्स का वर्गीकरण
| क्र. सं. | कार्बन परमाणुओं की संख्या के आधार पर मोनोसैकेराइड्स की श्रेणी | क्रियात्मक समूहों के आधार पर मोनोसैकेराइड्स की श्रेणी | |
|---|---|---|---|
| ऐल्डोस | कीटोस | ||
| 1. | ट्रायोस $\left(\mathrm{C}_3 \mathrm{H}_6 \mathrm{O}_3\right)$ | ग्लिसरैल्डिहाइड (एक ऐल्डोट्रायोस) | डाइहाइड्रॉक्सीएसीटोन (एक कीटोट्रायोस) |
| 2. | टेट्रोस $\left(\mathrm{C}_4 \mathrm{H}_8 \mathrm{O}_4\right)$ | एरिथ्रोस | एरिथ्रुलोस |
| 3. | पेंटोस $\left(\mathrm{C} _5 \mathrm{H} _{10} \mathrm{O} _5\right)$ | राइबोस | राइब्युलोस |
| 4. | हेक्सोस $\left(\mathrm{C} _6 \mathrm{H} _{12} \mathrm{O} _6\right)$ | ग्लूकोस | फ्रक्टोस |
2. ओलिगोसैकेराइड्स
परंपरागत रूप से, ओलिगोसैकेराइड्स ऐसे कार्बोहाइड्रेट होते हैं जिनमें दो से दस मोनोसैकेराइड इकाइयाँ ग्लाइकोसिडिक बंध द्वारा जुड़ी होती हैं। कुछ सामान्यतः पाए जाने वाले ओलिगोसैकेराइड्स माल्टोस, लैक्टोस, सुक्रोस आदि हैं।
3. पॉलीसैकेराइड्स
पॉलिसैकेराइड दस या अधिक मोनोसैकेराइड इकाइयों के ग्लाइकोसिडिक लिंकेज द्वारा जुड़े हुए बहुलक होते हैं। इन्हें कई तरीकों से वर्गीकृत किया जाता है जैसे कि दोहराने वाली मोनोसैकेराइड इकाई के प्रकार के आधार पर (होमो- और हेटरो-पॉलिसैकेराइड); शाखाओं की डिग्री के आधार पर; और मोनोमेरिक इकाइयों के बीच ग्लाइकोसिडिक लिंकेज के प्रकार के आधार पर। कुछ सामान्य पॉलिसैकेराइडों के उदाहरण हैं स्टार्च, ग्लाइकोजन, सेलुलोज और काइटिन।
कार्बोहाइड्रेट प्रोटीन और लिपिड से संयुक्त होकर ग्लाइकोकॉन्जुगेट्स बना सकते हैं। ग्लाइकोकॉन्जुगेट्स के तीन प्रकार होते हैं; ग्लाइकोप्रोटीन, प्रोटियोग्लाइकन और ग्लाइकोलिपिड। यदि कार्बोहाइड्रेट और प्रोटीन के संयोजन में प्रोटीन घटक प्रमुख हो, तो इसे ग्लाइकोप्रोटीन कहा जाता है। यदि संयोजन में प्रोटीन की तुलना में कार्बोहाइड्रेट की मात्रा अधिक हो, तो इसे प्रोटियोग्लाइकन कहा जाता है। जब कार्बोहाइड्रेट लिपिड से संयुक्त होता है, तो इसे ग्लाइकोलिपिड कहा जाता है।
(B) कार्बोहाइड्रेट की संरचना और गुण
(a) मोनोसैकेराइड
कुछ सामान्य मोनोसैकेराइडों की संरचना (चित्र 3.1) में दी गई है। मोनोसैकेराइड जैसे ग्लूकोज दोनों रूपों में मौजूद होता है

चित्र 3.1: कुछ मोनोसैकेराइडों की संरचना
सीधी श्रृंखला संरचना और चक्रीय संरचना (चित्र 3.2)। चक्रीय संरचनाएं कार्बोनिल समूह और हाइड्रॉक्सिल समूह के बीच अंतःअणुकीय अभिक्रिया द्वारा हेमीएसिटल निर्माण का परिणाम होती हैं।

चित्र 3.2: ग्लूकोज की संरचना: (a) सीधी श्रृंखला और (b) चक्रीय रूप
सभी मोनोसैकेराइड्स, डाइहाइड्रॉक्सी ऐसीटोन को छोड़कर, एक या अधिक असममित (काइरल) कार्बन (चार भिन्न समूहों से बंधे कार्बन परमाणु) रखते हैं, इसलिए ये प्रकाशिक रूप से सक्रिय समावयवी (एनैंटियोमर्स) होते हैं। एक अणु जिसमें $n$ काइरल केंद्र हों, उसके $2^{\mathrm{n}}$ स्टीरियोसोमर हो सकते हैं। इस प्रकार, एक काइरल केंद्र वाले ग्लिसरैल्डिहाइड के $2^{1}=2$ और चार काइरल केंद्रों वाले ग्लूकोज के $2^{4}=16$ स्टीरियोसोमर होते हैं।
$-OH$ समूह की अभिविन्यासता, जो कार्बोनिल कार्बन से सबसे दूर स्थित है, यह निर्धारित करती है कि वह शर्करा D या L शर्कराओं में से किस श्रेणी की है। जब यह $-OH$ समूह उस कार्बन परमाणु पर जिससे वह बंधा है, दाईं ओर होता है, तो वह शर्करा D-समावयवी होती है, और जब यह बाईं ओर होता है, तो वह L समावयवी होती है (चित्र 3.3)। जैविक तंत्र में मौजूद अधिकांश शर्कराएँ D शर्कराएँ होती हैं।

चित्र 3.3: ग्लूकोज के L और D रूप
मोनोसैकेराइड के समावयवी रूप जो केवल अपने हेमीएसिटल (एक मोनोसैकेराइड की ऐल्कोहॉलिक और ऐल्डिहाइड समूहों की अभिक्रिया से बना) या हेमीकीटल (एक मोनोसैकेराइड की ऐल्कोहॉलिक और कीटो समूहों की अभिक्रिया से बना) कार्बन परमाणु के बारे में अपनी विन्यास में भिन्न होते हैं, एनोमर कहलाते हैं। कार्बोनिल कार्बन परमाणु को एनोमेरिक कार्बन कहा जाता है। $\alpha$-एनोमर में, कार्बन का - $\mathrm{OH}$ समूह चीनी रिंग पर $\mathrm{CH}_{2} \mathrm{OH}$ समूह के विपरीत होता है जो कि काइरल केंद्र पर $\mathrm{D}$ और $\mathrm{L}$ विन्यास को निर्दिष्ट करता है (ग्लूकोज के मामले में $\mathrm{C}-5$)। दूसरा एनोमर $\beta$-एनोमर के रूप में जाना जाता है।
जलीय विलयन में $\alpha$ और $\beta$ एनोमरों का आपसी रूपांतरण म्यूटारोटेशन कहलाता है, जिसमें एक रिंग रूप संक्षेप में रेखीय रूप में खुलता है, फिर पुनः बंद होकर $\beta$ एनोमर उत्पन्न करता है (चित्र 3.4)।

चित्र 3.4: ग्लूकोज के दो चक्रीय रूप
जिन समावयवियों में केवल एक कार्बन परमाणु पर $-\mathrm{OH}$ की भिन्न विन्यास होती है, उन्हें एपिमर कहा जाता है। ग्लूकोज के सबसे महत्वपूर्ण एपिमर मैनोज (C-2 पर एपिमर) और गैलेक्टोज (C-4 पर एपिमर) हैं, जैसा कि आकृति 3.5 में दिखाया गया है।

आकृति 3.5: ग्लूकोज के एपिमर
(b) डाइसैकेराइड
डाइसैकेराइड दो मोनोसैकेराइडों से ग्लाइकोसिडिक बंध द्वारा जुड़े होते हैं। डाइसैकेराइड माल्टोज में दो D-ग्लूकोज अवशेष ग्लाइकोसिडिक बंध द्वारा जुड़े होते हैं, जो एक सहसंयोजी बंध है जो एक मोनोसैकेराइड के $-\mathrm{OH}$ समूह को दूसरे शर्करा इकाई के ऐनोमेरिक कार्बन से जोड़कर बनता है। लैक्टोज D-गैलेक्टोज और D-ग्लूकोज अवशेषों से बना होता है (आकृति 3.6 और 3.7)।
डाइसैकेराइड को तनु अम्ल के साथ उबालकर उनके घटक मोनोसैकेराइडों में विघटित किया जा सकता है। सुक्रोज के जल-विघटन से ग्लूकोज और फ्रुक्टोज का मिश्रण प्राप्त होता है।

आकृति 3.6: दो $\alpha$ D-ग्लूकोज अणुओं से माल्टोज का निर्माण
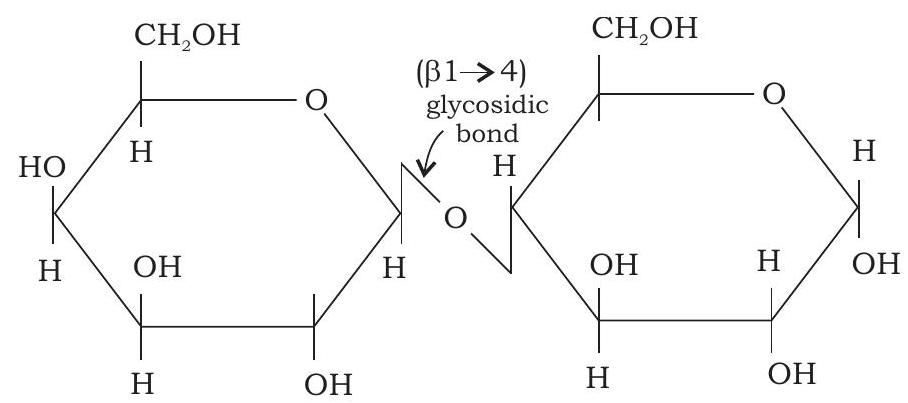
लैक्टोज़ (β-D-गैलैक्टोपाइरानोसिल-(1→4) α-D-ग्लूकोपाइरानोज़)
आकृति 3.7: लैक्टोज़ की संरचना
(c) बहुशर्कराएँ
कार्यात्मक भूमिकाओं के आधार पर समबहुशर्कराओं को भंडारण बहुशर्कराएँ और संरचनात्मक बहुशर्कराएँ में विभाजित किया जाता है। भंडारण बहुशर्कराएँ मोनोशर्करा के भंडारण रूप के रूप में कार्य करती हैं जिन्हें ईंधन के रूप में उपयोग किया जाता है। स्टार्च पौधों में भंडारण बहुशर्करा का उदाहरण है, और ग्लाइकोजन जानवरों में भंडारण बहुशर्करा है। संरचनात्मक बहुशर्कराएँ जैसे सेल्यूलोज़ और काइटिन क्रमशः पौधे की कोशिका भित्ति और जानवरों के बाह्यकंकाल में संरचनात्मक तत्वों के रूप में कार्य करते हैं। विषमबहुशर्कराएँ, समबहुशर्कराओं के विपरीत, जीवों के बाह्यकोशिकीय समर्थन प्रदान करती हैं। जानवरों के ऊतकों के बाह्यकोशिकीय स्थान में ये एक आधात्रिक बनाते हैं जो व्यक्तिगत कोशिकाओं को एक साथ रखता है और कोशिकाओं तथा ऊतकों को आकृति, समर्थन और सुरक्षा प्रदान करता है। कुछ समबहुशर्कराओं के नाम और गुणधर्म सारणी 3.2 में दिए गए हैं।
सारणी 3.2: कुछ सामान्य समबहुशर्कराओं की सूची
| नाम | घटक मोनोसैकेराइड | आकार (मोनोसैकेराइड अवशेषों की संख्या) | जैविक महत्व |
|---|---|---|---|
| स्टार्च | a-D-ग्लूकोज | $50-5000$ तक $10^{6}$ | पौधों में ऊर्जा का भंडारण |
| ग्लाइकोजन | a-D-ग्लूकोज | 50000 तक | जीवाणुओं और जानवरों में ऊर्जा का भंडारण |
| सेलुलोज | $\beta$-D-ग्लूकोज | 15000 तक | यह संरचनात्मक भूमिका निभाता है और कोशिका भित्ति को कठोरता और मजबूती प्रदान करता है। |
| काइटिन | $\beta$-N-एसिटिल-D-ग्लूकोसामिन | बहुत बड़ा | यह संरचनात्मक भूमिका निभाता है और कीटों के बाहरी कंकाल को कठोरता प्रदान करता है। |
| इनुलिन | $\beta$-D-फ्रुक्टोज | $30-35$ | पौधों में ऊर्जा का भंडारण। |
| पेक्टिन | a-D-गैलेक्टूरोनिक अम्ल | - | इसकी संरचनात्मक भूमिका है: यह पौधे की कोशिका भित्तियों में सेलुलोज फाइब्रिल्स को एक साथ रखता है। |
| डेक्सट्रान | a-D-ग्लूकोज | विस्तृत सीमा | यह जीवाणुओं में बाह्यकोशिकीय चिपचिपे के रूप में संरचनात्मक भूमिका निभाता है। |
| ज़ाइलन | $\beta$-D-ज़ाइलोज | $30-100$ | इसकी पौधों में भंडारण और सहायक भूमिकाएँ हैं। |
कुछ सामान्य पॉलीसैकेराइडों के उदाहरण
(a) स्टार्च
स्टार्च पौधों में ट्यूबर, बीज, फल और जड़ों में आरक्षित कार्बोहाइड्रेट के रूप में पाया जाता है। यह दो समबहुलबहुल-पॉलिसैकेराइडों, एमिलोज़ (15-20\%) और एमिलोपेक्टिन $(80-85 \%)$ से बना होता है। एमिलोज़ α-D-ग्लूकोज़ मोनोमरों का रैखिक बहुलक है और यह $\mathrm{a}(1 \rightarrow 4)$ बंधों द्वारा जुड़ा होता है (चित्र 3.8)। दूसरी ओर, एमिलोपेक्टिन में ग्लूकोज़ इकाइयाँ एमिलोज़ की तरह $\mathrm{a}(1 \rightarrow 4)$ ग्लाइकोसिडिक बंधों द्वारा जुड़ी होती हैं। हालाँकि, एमिलोज़ के विपरीत, यह अत्यधिक शाखित होता है। शाखा बिंदु हर 24 से 30 ग्लूकोज़ अवशेषों पर होते हैं और शाखा बिंदुओं पर बंध $\mathrm{a}(1 \rightarrow 6)$ ग्लाइकोसिडिक होता है (चित्र 3.9)। आयोडीन के साथ स्टार्च का विशिष्ट नीला रंग एमिलोज़ के कारण होता है। इसके विपरीत, एमिलोपेक्टिन आयोडीन के साथ केवल फीका लाल-भूरा रंग देता है। लार में मौजूद एंजाइम (लार एमिलेज़) और अग्न्याशयी रस में मौजूद एंजाइम (अग्न्याशयी एमिलेज़) स्टार्च के $\mathrm{a}(1 \rightarrow 4)$ ग्लाइकोसिडिक बंधों को जल-अपघटित करते हैं और इस प्रकार इसे मोनोमेरिक ग्लूकोज़ अवशेषों में पचाते हैं।
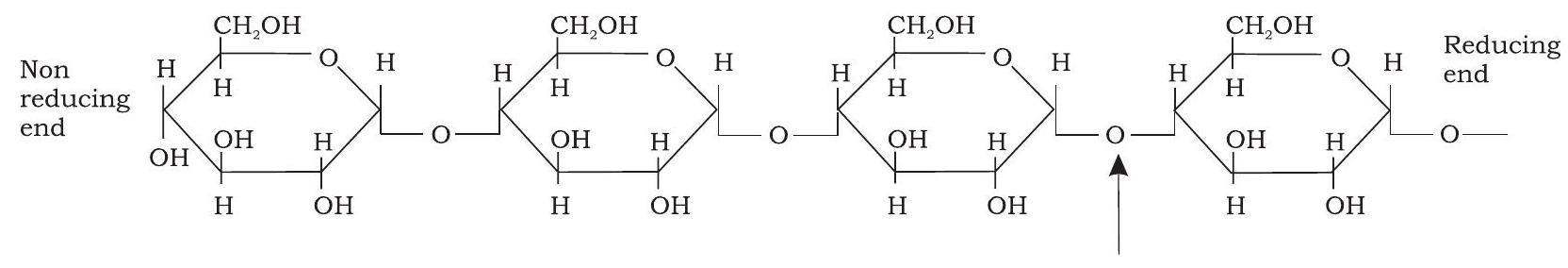
$\hspace{8cm}\alpha(1 \rightarrow 4)$ ग्लाइकोसिडिक बंध
चित्र 3.8: एमिलोज़ की संरचना
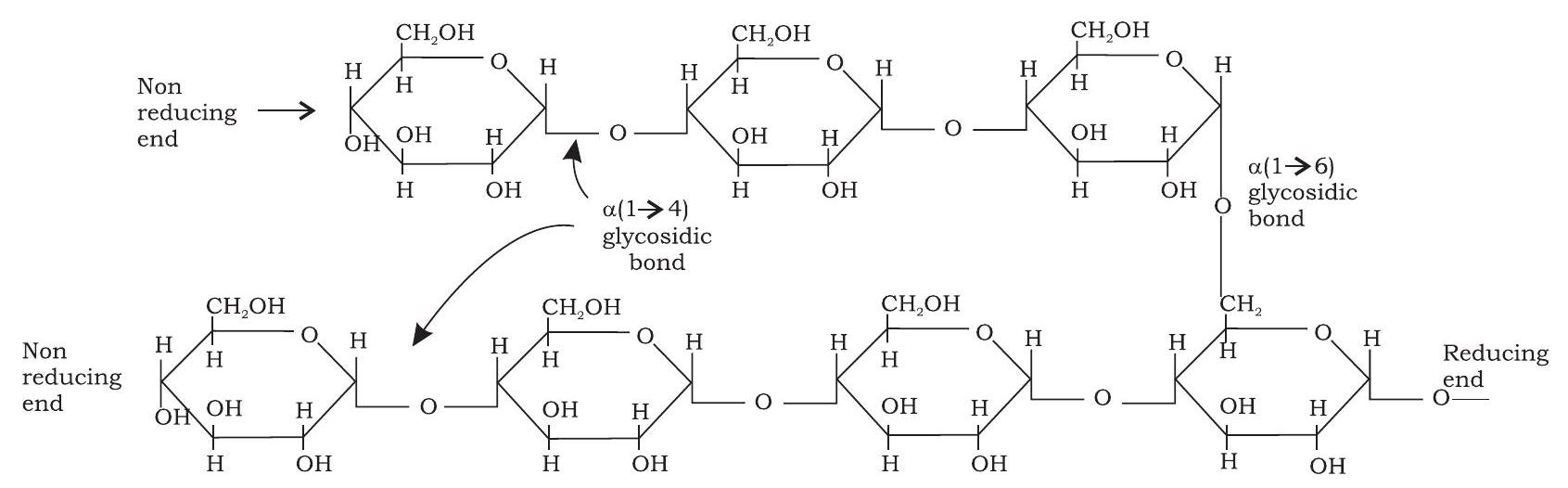
आकृति 3.9: एमिलोपेक्टिन की संरचना
(b) ग्लाइकोजन
ग्लाइकोजन एक अत्यधिक शाखित संग्रहणी होमोपॉलिसैकेराइड है जो जानवरों में पाया जाता है। एमिलोपेक्टिन के समान, यह ग्लूकोज इकाइयों से बना होता है जो $\mathrm{a}(1 \rightarrow 4)$ ग्लाइकोसिडिक लिंकेज द्वारा जुड़ी होती हैं और शाखा बिंदुओं पर $\alpha(1 \rightarrow 6)$ लिंकेज होती है। पेशीय कोशिकाओं में ग्लाइकोजन उनके शुष्क भार का 1-2 प्रतिशत होता है, और यकृत कोशिकाओं में ग्लाइकोजन उनके शुष्क भार का 10 प्रतिशत तक होता है।
(c) सेल्युलोज
सेल्युलोज पौधों में पाया जाने वाला सबसे प्रचुर बाह्य-कोशिकीय संरचनात्मक पॉलिसैकेराइड है। यह जैवमंडल में सभी जैवअणुओं में सबसे प्रचुर है। यह पौधे की कोशिका भित्ति का प्राथमिक संरचनात्मक घटक है। संरचनात्मक रूप से, सेल्युलोज 15000 तक D-ग्लूकोज इकाइयों का एक रैखिक बहुलक है जो $\beta(1 \rightarrow 4)$ ग्लाइकोसिडिक बंधों द्वारा जुड़ी होती हैं (आकृति 3.10)। स्टार्च के विपरीत, सेल्युलोज को मनुष्य पचा नहीं सकता क्योंकि मानव आंत्र में $\beta(1 \rightarrow 4)$ ग्लाइकोसिडिक बंध को हाइड्रोलाइज़ करने वाला एंजाइम सेल्युलेज नहीं होता है। हालांकि, मवेशी और दीमक सेल्युलोज को पचा सकते हैं क्योंकि उनके आंत्र में सहजीवी सूक्ष्मजीव होते हैं जो सेल्युलेज स्रावित करते हैं जो सेल्युलोज को हाइड्रोलाइज़ करके पचाता है।
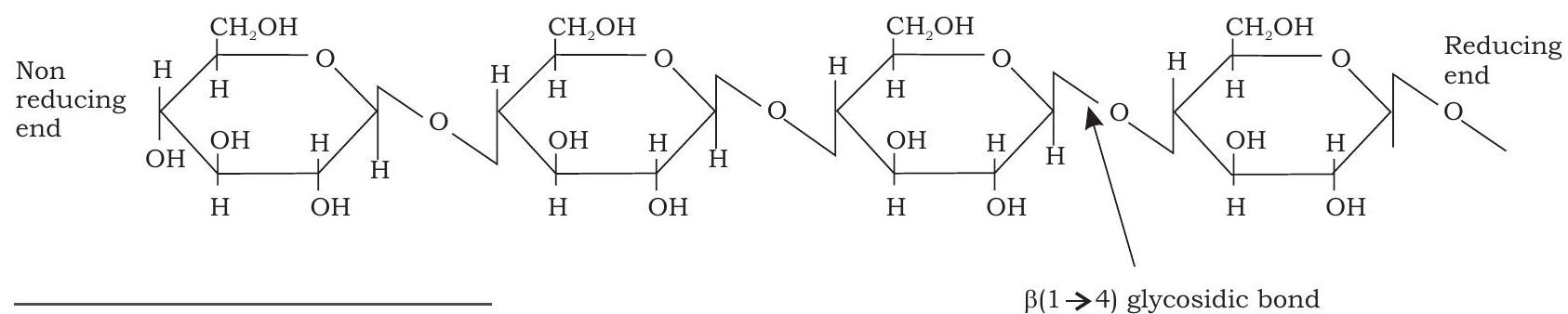
चित्र 3.10: सेलुलोज की संरचना
(d) काइटिन
काइटिन $\beta(1 \rightarrow 4)$ से जुड़े $\mathrm{N}$-एसिटिल-डी-ग्लूकोसामिन अवशेषों का एक रैखिक पॉलीसैकेराइड है। यह अकशेरुकी जीवों (क्रस्टेशियंस, कीड़े और मकड़ियों) के बाह्य कंकाल का मुख्य संरचनात्मक घटक है और अधिकांश कवकों की कोशिका भित्ति का मुख्य घटक है। काइटिन और सेलुलोज की संरचनाएं समान हैं, सिवाय इसके कि सेलुलोज में दूसरी कार्बन स्थिति पर स्थित $\mathrm{OH}$ समूह काइटिन में एक एसिटामिडो समूह से प्रतिस्थापित हो जाता है। $\mathrm{N}$-एसिटिल साइड श्रृंखलाओं का व्यापक हाइड्रोजन बंधन काइटिन को कठोर और अघुलनशील पॉलिमर बनाता है।
(e) पेप्टिडोग्लाइकन
पेप्टिडोग्लाइकन जीवाणु कोशिका भित्ति का कठोर घटक बनाता है। यह बारी-बारी से $\beta(1 \rightarrow 4)$ से जुड़े $\mathrm{N}$-एसिटिल-डी-ग्लूकोसामिन (NAG) और $\mathrm{N}$-एसिटिल म्यूरामिक एसिड (NAM) अवशेषों का एक विषमपॉलीसैकेराइड है। रैखिक पॉलीसैकेराइड श्रृंखलाओं को $\mathrm{N}$-एसिटिल म्यूरामिक एसिड से जुड़े छोटे पेप्टाइडों द्वारा पार-बंधित किया जाता है। पेप्टाइड द्वारा पार-बंधन पॉलीसैकेराइड श्रृंखलाओं को एक मजबूत आवरण में जोड़ता है जो संपूर्ण कोशिका को घेरता है और कोशिका की परासरणी फटन को रोकता है।
लाइसोज़ाइम, जो मानव आँसुओं में मौजूद एक एंजाइम है, पेप्टिडोग्लाइकन के $\beta(1 \rightarrow 4)$ ग्लाइकोसिडिक बंधन को हाइड्रोलाइज़ करके जीवाणुओं को मारता है।
बॉक्स 1
एगर
एगर एक जेलनुमा हेटरोपॉलिसैकेराइड है जो समुद्री लाल शैवालों जैसे Gelidium, Gracilaria, Gigartina आदि प्रजातियों की कोशिका भित्ति में उत्पन्न होता है। यह सल्फेटेड हेटरोपॉलिसैकेराइड्स का मिश्रण है जो D-गैलेक्टोज़ और L-गैलेक्टोज़ व्युत्पन्नों से बना होता है जो C3 और C6 के बीच ईथर लिंक से जुड़े होते हैं। एगरोज़ वह एगर घटक है जिसमें बहुत कम आवेशित समूह (सल्फेट्स, पाइरुवेट्स) होते हैं। इसका आण्विक भार 80,000-1,40,000 की सीमा में होता है। यदि एगर और एगरोज़ को गर्म पानी में घोला जाए तो वे विलयन बनाते हैं जो ठंडा होने पर जेल में बदल जाता है। एगरोज़ जेल न्यूक्लिक अम्लों के विद्युत्क्रिय वियोजन के लिए निष्क्रिय आधार के रूप में प्रयुक्त होते हैं। एगर जीवाणुओं और पादप ऊतक संवर्धन के विकास के लिए सतह बनाने में प्रयुक्त होता है।
3.2 फैटी एसिड और लिपिड्स
लिपिड्स जैविक यौगिकों का एक समूह है जो जीवित जीवों में पाए जाते हैं। ये अपनी संरचनाओं और कार्यों में भिन्न होते हैं। अपने हाइड्रोफोबिक और अध्रुवीय स्वभाव के कारण, लिपिड्स कार्बनिक विलायकों में घुलनशील होते हैं। लिपिड्स मुख्य रूप से हाइड्रोकार्बन श्रृंखलाओं से बने होते हैं जो ग्लिसरॉल से एस्टर लिंकेज के माध्यम से जुड़े होते हैं। हम लिपिड्स को दो श्रेणियों में व्यापक रूप से वर्गीकृत करते हैं—सरल लिपिड्स और यौगिक लिपिड्स। इन दो प्रमुख लिपिड श्रेणियों के भीतर विभिन्न प्रकार के लिपिड्स शामिल होते हैं। इनमें वसा, ट्रायसिलग्लिसरॉल्स, मोम, फॉस्फोलिपिड्स, स्टेरॉयड आदि शामिल हैं।
वसा के जल-अपघटन के परिणामस्वरूप फैटी अम्ल प्राप्त होते हैं। प्राकृत रूप से उपस्थित फैटी अम्ल सामान्यतः दो कार्बन इकाइयों से संश्लेषित होते हैं और इसलिए सम संख्या में कार्बन परमाणु रखते हैं (चित्र 3.11)। 2 कार्बन इकाइयों से संश्लेषित फैटी अम्ल श्रृंखला संतृप्त (कोई द्विबंध नहीं) या असंतृप्त (एक या अधिक द्विबंध) हो सकती है (तालिका 3.3)।

चित्र 3.11: फैटी अम्ल (स्टीयरिक अम्ल) की संरचना
फैटी अम्लों को कुल कार्बन संख्या के बाद कोलन (:) और फिर कुल द्विबंध संख्या के साथ $\Delta$ (डेल्टा) द्वारा दर्शाया जाता है, जिसमें अभिगृहित संख्या कोष्ठक में द्विबंध की स्थिति को परिभाषित करती है। उदाहरण के लिए, एक फैटी अम्ल जिसमें 18 कार्बन हैं और दो द्विबंध C-9 और $\mathrm{C}-10$ तथा $\mathrm{C}-12$ और $\mathrm{C}-13$ के बीच हैं, उसे 18:2 $(\left.\Delta^{9,12}\right)$ के रूप में दर्शाया जाएगा। असंतृप्त फैटी अम्ल असंतृप्तता की डिग्री के आधार पर दो प्रकार के होते हैं:
एकल-असंतृप्त फैटी अम्ल: ‘मोनो’ का अर्थ एकल। इसलिए, एकल-असंतृप्त फैटी अम्ल में केवल एक ही द्विबंध होता है। उदाहरण के लिए, ओलेइक अम्ल (चित्र 3.12)।

चित्र 3.12: असंतृप्त फैटी अम्ल (ओलेइक अम्ल) की संरचना
बहु-असंतृप्त वसा अम्ल: जैसा कि नाम से स्पष्ट है, इन वसा अम्लों में एक से अधिक द्विबंध होते हैं। उदाहरणस्वरूप, लिनोलिक अम्ल में दो द्विबंध होते हैं, लिनोलेनिक अम्ल में तीन द्विबंध होते हैं; और अरैकिडोनिक अम्ल में चार द्विबंध होते हैं।
तालिका 3.3: संतृप्त और असंतृप्त वसा अम्लों के कुछ उदाहरण जिनमें श्रृंखला लंबाई और गलनांक दर्शाया गया है
| सामान्य नाम | प्रतीक | कार्बनों की संख्या | गलनांक |
|---|---|---|---|
| संतृप्त | |||
| लॉरिक अम्ल | $12: 0$ | 12 | $44^{\circ} \mathrm{C}$ |
| मिरिस्टिक अम्ल | $14: 0$ | 14 | $58^{\circ} \mathrm{C}$ |
| पामिटिक अम्ल | $16: 0$ | 16 | $63^{\circ} \mathrm{C}$ |
| स्टीयरिक अम्ल | $18: 0$ | 18 | $69^{\circ} \mathrm{C}$ |
| अरैकिडिक अम्ल | $20: 0$ | 20 | $77^{\circ} \mathrm{C}$ |
| असंतृप्त | |||
| पामिटोलिक अम्ल | $16: 1\left(\Delta^{9}\right)$ | 16 | $0^{\circ} \mathrm{C}$ |
| ओलिक अम्ल | $18: 1\left(\Delta^{9}\right)$ | 18 | $13^{\circ} \mathrm{C}$ |
| लिनोलिक अम्ल | $18: 2\left(\Delta^{9, 12}\right)$ | 18 | $-5^{\circ} \mathrm{C}$ |
| अरैकिडोनिक अम्ल | $20: 4\left(\Delta^{5,8,11,14}\right)$ | 20 | $-49^{\circ} \mathrm{C}$ |
लिपिडों का वर्गीकरण
1. सरल लिपिड
एक सरल लिपिड विभिन्न अल्कोहलों के साथ कोई अन्य समूह न रखने वाला वसा अम्ल एस्टर होता है। उदाहरण के लिए, वसाएँ और मोम।
(a) ट्रायसिलग्लिसरॉल्स: इन्हें व्यापक रूप से ट्राइग्लिसराइड्स (या तटस्थ वसा) के नाम से जाना जाता है। ये ग्लिसरॉल और फैटी एसिड के एस्टर होते हैं (चित्र 3.13)। वे ट्राइग्लिसराइड्स जिनकी तीनों एस्टर स्थितियों में एक ही फैटी एसिड होता है, सरल ट्राइग्लिसराइड्स कहलाते हैं। वे ट्राइग्लिसराइड्स जिनकी तीनों स्थितियों में एक से अधिक फैटी एसिड होते हैं, मिश्रित ट्राइग्लिसराइड्स कहलाते हैं। ट्रायसिलग्लिसरॉल शरीर को ऊर्जा देने के लिए आवश्यक है। ट्राइग्लिसराइड्स ऊर्जा भंडारण का मुख्य साधन हैं, विशेष रूप से वसा ऊतक में।

चित्र 3.13: ट्रायसिलग्लिसरॉल की संरचना
(b) मोम: मोम उच्च आण्विक भार वाले एकल-हाइड्रॉक्सी अल्कोहल के साथ फैटी एसिड के एस्टरीकरण से बनता है। मोम विभिन्न जीवों में पाया जाता है। उदाहरण के लिए, मोम जानवरों और पौधों की सतह पर सुरक्षात्मक परत के रूप में कार्य करता है और उष्णकटिबंधीय पौधों में जल हानि को कम करता है।
2. यौगिक लिपिड्स
यौगिक लिपिड्स फैटी एसिड और अल्कोहल के एस्टर होते हैं और इनमें अतिरिक्त समूह भी होते हैं। इन लिपिड्स के फैटी एसिड घटक जल-विरोधी पूंछ बनाते हैं, और अल्कोहल खंड सहित अतिरिक्त समूह जल-प्रेमी सिर बनाते हैं। इस प्रकार की संरचना को उभयधर्मी अणु कहा जाता है। यौगिक लिपिड्स के सामान्य उदाहरणों में फॉस्फोलिपिड्स और स्टेरॉयड्स शामिल हैं।
फॉस्फोलिपिड्स उभयधर्मी अणु होते हैं जो दो जल-विरोधी फैटी एसिड पूंछों और एक जल-अनुरागी फॉस्फेट समूह सिर से बने होते हैं। फॉस्फोलिपिड्स मुख्यतः कोशिका झिल्ली में पाए जाते हैं। ये यौगिक ग्लिसरॉल रीढ़ (ग्लिसरोफॉस्फोलिपिड्स) या स्फिंगॉइड आधार रीढ़ (स्फिंगोफॉस्फोलिपिड) से जुड़े फैटी एसिड श्रृंखलाओं से बने होते हैं (चित्र 3.14)। ग्लिसरोफॉस्फोलिपिड्स में एक संशोधित फॉस्फेट समूह ग्लिसरॉल के तीसरे कार्बन पर कब्जा करता है। एक फॉस्फोलिपिड को फॉस्फेट समूह से जुड़े संशोधक के प्रकार से परिभाषित किया जाता है। सबसे सामान्य कोलीन (फॉस्फेटिडिलकोलीन) और सेरीन (फॉस्फेटिडिलसेरीन) होते हैं। इसी प्रकार, स्फिंगोलिपिड्स के मामले में, जब सिर समूह में केवल एक हाइड्रोजन परमाणु होता है, तो इसे सेरामाइड कहा जाता है। कई बार, स्फिंगोलिपिड्स में सिर समूह फॉस्फोकोलीन हो सकता है, जिससे एक स्फिंगोमायलिन बनता है। स्फिंगोलिपिड्स में, फैटी एसिड श्रृंखला स्फिंगॉइड रीढ़ से एस्टर लिंकेज के बजाय एमाइड लिंकेज के माध्यम से जुड़ी होती है।
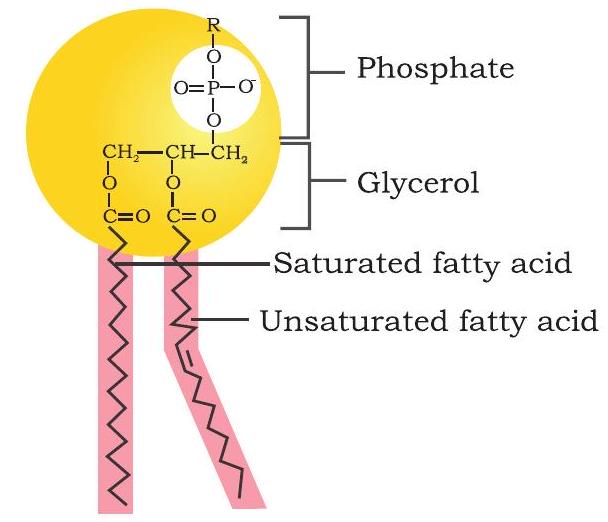
(क) ग्लिसरोफॉस्फोलिपिड
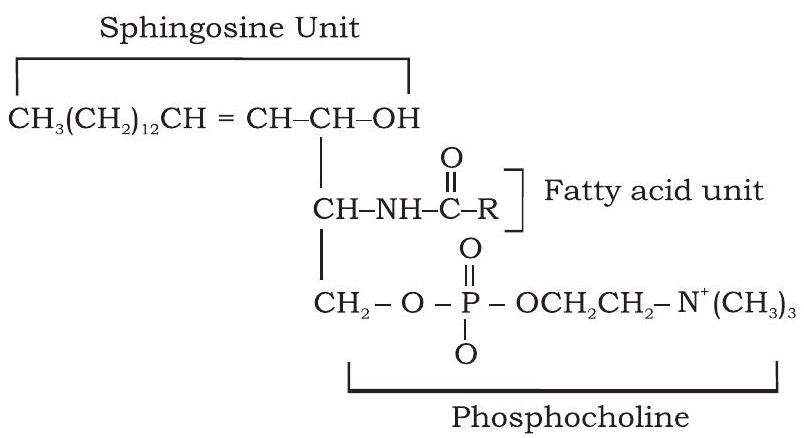
(ख) स्फिंगोफॉस्फोलिपिड
चित्र 3.14: (a) ग्लिसरोफॉस्फोलिपिड और (b) स्फिंगोफॉस्फोलिपिड की संरचना
फॉस्फोलिपिड स्वतः पानी के साथ मिश्रित नहीं होते। इसके बजाय, वे एक गोलाकार संरचना ग्रहण करते हैं जिसे मिसेल कहा जाता है।
स्टेरॉयड अन्य लिपिड से इस मामले में भिन्न होते हैं कि इनमें एक विशिष्ट चार-संलग्न वलय संरचना होती है। फिर भी, अब तक चर्चा किए गए अन्य सभी लिपिड की तरह, स्टेरॉयड भी जल-विरोधी प्रकृति के होते हैं और पानी में अविलेय होते हैं। कोशिका में स्टेरॉयड रिसेप्टर लिगैंड के रूप में कार्य करते हैं और चयापचय को नियंत्रित करने में सहायता करते हैं। कोलेस्ट्रॉल स्टेरॉयड का सबसे सामान्य व्युत्पन्न है (चित्र 3.15)।

चित्र 3.15: कोलेस्ट्रॉल की संरचना
मुख्यतः यकृत द्वारा संश्लेषित, कोलेस्ट्रॉल सभी स्टेरॉयड हार्मोन—जिनमें टेस्टोस्टेरोन और एस्ट्राडियोल शामिल हैं—का प्रमुख अग्रद्रव्य है। इसके अतिरिक्त, कोलेस्ट्रॉल अधिकांश यूकैरियोट्स की प्लाज्मा झिल्ली में भी पाया जाता है, जहाँ यह दृढ़ता प्रदान करता है। पादपों में पाए जाने वाले सामान्य स्टेरॉयड उदाहरण हैं फाइटोस्टेरॉल और स्टिग्मास्टेरॉल, जो झिल्ली की द्रवता और पारगम्यता को नियंत्रित करते हैं। अर्गोस्टेरॉल विटामिन D का एक महत्वपूर्ण अग्रद्रव्य है और सामान्यतः कवक में पाया जाता है।
3.3 अमीनो अम्ल
प्रोटीनों की इकाईयाँ अमीनो अम्ल, सामान्य सूत्र द्वारा दर्शाए जाते हैं:

जहाँ केंद्रीय कार्बन परमाणु को α-कार्बन कहा जाता है, जो चार विभिन्न समूहों से जुड़ा होता है; एक अम्लीय कार्बोक्सिलिक (- $\mathrm{COOH}$), एक क्षारीय अमीनो $\left(-\mathrm{NH}_2\right)$ समूह, एक हाइड्रोजन परमाणु, और एक $\mathrm{R}$ समूह जिसे साइड चेन कहा जाता है। केवल साइड चेन $\mathrm{R}$ ही सभी 20 अमीनो अम्लों में भिन्न होता है, यह ग्लाइसीन में एक साधारण हाइड्रोजन परमाणु $(\mathrm{H})$ जितना सरल हो सकता है या एलानिन में एक मेथिल $\left(-\mathrm{CH}_3\right)$ हो सकता है। कार्बोक्सिलिक समूह पहला कार्बन देता है, और जिस कार्बन परमाणु से कार्बोक्सिलिक समूह जुड़ा होता है उसे α-कार्बन कहा जाता है। चूँकि अधिकांश अमीनो अम्लों का α-कार्बन चार विभिन्न समूहों से टेट्राहेड्रल रूप से जुड़ा होता है, इसलिए अमीनो अम्लों का α-कार्बन काइरल या असममित होता है। इस असममित α-कार्बन के कारण, अमीनो अम्ल दो प्रकाशिक रूप से सक्रिय रूपों या दर्पण प्रतिबिंब रूपों में उपस्थित होते हैं (चित्र 3.16)।

चित्र 3.16: अमीनो अम्ल के L और D आइसोमर।
L आइसोमर में $-\mathrm{NH}_2$ समूह α-कार्बन के बाईं ओर होता है और D आइसोमर में $-\mathrm{NH}_2$ समूह α-कार्बन के दाईं ओर होता है। प्रोटीनों में केवल L आइसोमर के अमीनो अम्ल पाए जाते हैं, D आइसोमर जैविक प्रोटीन में दुर्लभ होते हैं। 20 मानक अमीनो अम्लों की सूची तालिका 3.4 में दी गई है। 20 अमीनो अम्लों की संरचना चित्र 3.17 से 3.21 तक दी गई है।
तालिका 3.4: 20 मानक अमीनो अम्ल उनके तीन अक्षर और एक अक्षर प्रतीक के साथ
| अमीनो अम्ल | संक्षिप्त प्रतीक (तीन अक्षर) | एकल अक्षर प्रतीक |
|---|---|---|
| ध्रुवीय, अनआवेशित R समूह | ||
| सीरिन | Ser | $\mathrm{S}$ |
| थ्रियोनिन | Thr | $\mathrm{T}$ |
| सिस्टीन | Cys | $\mathrm{C}$ |
| एस्पैरेजिन | Asn | $\mathrm{N}$ |
| ग्लूटामिन | Gln | $\mathrm{Q}$ |
| अरोमैटिक R समूह | ||
| फ़ेनिलएलानिन | Phe | $\mathrm{F}$ |
| ट्रिप्टोफ़ैन | Trp | $\mathrm{W}$ |
| टायरोसिन | Tyr | $\mathrm{Y}$ |
| अध्रुवीय ऐलिफैटिक अमीनो अम्ल | ||
| ग्लाइसिन | Gly | G |
| वैलिन | Val | $\mathrm{V}$ |
| एलानिन | Ala | A |
| प्रोलिन | Pro | $\mathrm{P}$ |
| ल्यूसिन | Leu | $\mathrm{L}$ |
| आइसोल्यूसिन | Ile | $\mathrm{I}$ |
| मेथिओनिन | Met | $\mathrm{M}$ |
| धनात्मक आवेश (क्षारकीय) R समूह | ||
| लाइसिन | Lys | $\mathrm{K}$ |
| आर्जिनिन | Arg | $\mathrm{R}$ |
| हिस्टिडिन | His | $\mathrm{H}$ |
| ऋणात्मक आवेश (अम्लीय) R समूह | ||
| एस्पार्टेट | Asp | $\mathrm{D}$ |
| ग्लूटामेट | Glu | $\mathrm{E}$ |

चित्र 3.17: ध्रुवीय अनआवेशित अमीनो अम्लों की संरचना

चित्र 3.18: धनात्मक आवेश वाले अमीनो अम्लों की संरचना

चित्र 3.19: अध्रुवीय ऐलिफैटिक अमीनो अम्लों की संरचना

चित्र 3.20: एरोमैटिक अमीनो अम्लों की संरचना

चित्र 3.21: ऋणात्मक आवेशित अमीनो अम्लों की संरचना
नामकरण
अमीनो अम्लों में कार्बन की संख्या ग्रीक अक्षरों का प्रयोग करके की जाती है। $\mathrm{R}$ समूह में $\alpha$-कार्बन से जुड़े अतिरिक्त कार्बनों को $\beta$ (बीटा), $\gamma$ (गामा), $\delta$ (डेल्टा), $\varepsilon$ (एप्सिलॉन) आदि नाम दिए जाते हैं और ये $\alpha$-कार्बन से बाहर की ओर बढ़ते हैं। अन्य कार्बनिक अणुओं की तरह, कार्बन परमाणुओं की संख्या कार्बोक्सिलिक समूह से प्रारंभ होती है और कार्बोक्सिलिक कार्बन $\mathrm{C}-1$ होता है तथा $\alpha$-कार्बन $\mathrm{C}-2$ होगा (चित्र 3.22)।
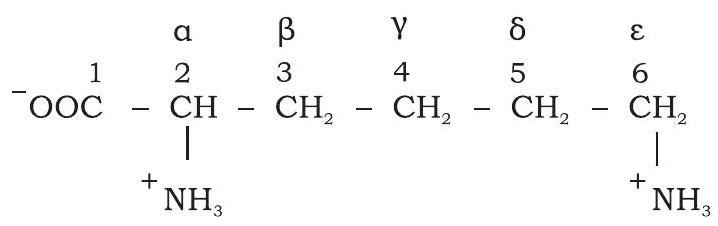
चित्र 3.22: L-लाइसिन के कार्बन परमाणुओं की संख्या
अमीनो अम्लों की विद्युत-रासायनिक गुणधर्म
अनुवाद (हिन्दी):
शारीरिक pH (pH = 7) पर अमीनो अम्लों का α-COOH समूह तथा α-NH₂ समूह विलयन में आयनित (प्रोटॉन हटकर) होकर क्रमशः -COO⁻ (ऋण आवेश) तथा -⁺NH₃ (धन आवेश) बनाते हैं। अमीनो अम्लों की इस द्विध्रुवीय अवस्था को ‘ज़्विटरायन’ कहते हैं। यह अवस्था कार्बॉक्सिल समूह से प्रोटॉन के अमीनो समूह में स्थानांतरित होने के कारण उत्पन्न होती है (चित्र 3.23)।

चित्र 3.23: ग्लाइसीन का ज़्विटरायन
गैर-मानक तथा गैर-प्रोटीन अमीनो अम्ल
कुछ अमीनो अम्ल गैर-मानक होते हैं। ये कोशिकाओं में स्वाभाविक रूप से उपस्थित होते हैं, परंतु प्रोटीन संश्लेषण में भाग नहीं लेते। ये विशिष्ट मानक अमीनो अम्लों के संशोधन के बाद प्रोटीन संश्लेषणोपरांत उत्पन्न होते हैं। उदाहरण—4-हाइड्रॉक्सीप्रोलिन (प्रोलिन का हाइड्रॉक्सिलीकरण), 5-हाइड्रॉक्सीलाइसिन, सेलेनोसिस्टीन तथा γ-कार्बॉक्सीग्लूटामिक अम्ल। जो अमीनो अम्ल प्रोटीन का हिस्सा नहीं होते, वे विभिन्न पादपों, प्राणियों व सूक्ष्मजीवों में व्यापक रूप से पाए जाते हैं; इन्हें ‘गैर-प्रोटीन अमीनो अम्ल’ कहते हैं। कुछ उदाहरण हैं—L-ऑर्निथिन, L-सिट्रुलिन, β-अलानिन, क्रिएटिन तथा γ-अमीनोब्यूटिरेट।
3.4 प्रोटीन संरचना
प्रोटीन सभी कोशिकाओं में मौजूद सबसे प्रचुर मैक्रोमोलेक्यूल हैं, जो सबसे सरल जीवाणुओं से लेकर मनुष्यों और पौधों तक में पाए जाते हैं। प्रोटीन मैक्रोमोलेक्यूल्स का सबसे विविध समूह है; एक एकल कोशिका में हजारों भिन्न-भिन्न प्रोटीन मौजूद हो सकते हैं। प्रोटीन 20 प्राकृतिक अमीनो अम्लों से बने होते हैं, जो एक दूसरे से कोवैलेंट बंधन द्वारा जुड़कर रेखीय क्रम बनाते हैं। सबसे उल्लेखनीय बात यह है कि कोशिकाएं इन 20 अमीनो अम्लों को अनेक विभिन्न संयोजनों में जोड़कर पूरी तरह से भिन्न संरचना और गुणों वाले प्रोटीन बना सकती हैं। इन बिल्डिंग ब्लॉकों से जीव कैटेलिस्ट (एंजाइम), एंटीबॉडी, ट्रांसपोर्टर, हार्मोन, ट्रांसक्रिप्शन फैक्टर, मांसपेशी रेशे, झिल्ली प्रोटीन आदि की विशाल विविधता उत्पन्न कर सकते हैं। ये उत्पाद सभी जीवनदायी प्रक्रियाओं में भाग लेते हैं, जैसे प्रत्येक कोशिका तक ऑक्सीजन और पोषक तत्वों का परिवहन, मांसपेशी संकुचन, तंत्रिका आवेग का संचरण, चयापचय का नियंत्रण, वृद्धि और विभेदन, यांत्रिक सहारा प्रदान करना, प्रतिरक्षा प्रतिक्रिया, सिग्नल ट्रांसडक्शन और भी बहुत कुछ।
अमीनो अम्लों की संरचना और उनका प्रोटीन में क्रम प्रोटीन की संरचना को निर्धारित करता है। प्रोटीन संरचनाओं के चार स्तर—प्राथमिक, द्वितीयक, तृतीयक और चतुष्कोणीय—वर्णित किए गए हैं। प्राथमिक संरचना एक ऐसा अमीनो अम्लों का क्रम है जो पेप्टाइड बॉन्ड नामक सहसंयोजी बंध से जुड़े होते हैं। द्वितीयक संरचना एक विशिष्ट अवशेष पैटर्न आधारित स्थिर संरचना है, जबकि तृतीयक संरचना में पॉलीपेप्टाइड्स का त्रि-आयामी वलयन होता है। चतुष्कोणीय संरचना दो या अधिक पॉलीपेप्टाइड उप-इकाइयों का सम्मिलित समुच्चय होता है।
3.4.1 प्रोटीन की प्राथमिक संरचना
प्रोटीन की प्राथमिक संरचना वह रैखिक श्रृंखला है जिसमें अमीनो अम्ल क्रम पेप्टाइड बंधों से जुड़े होते हैं (चित्र 3.24)।
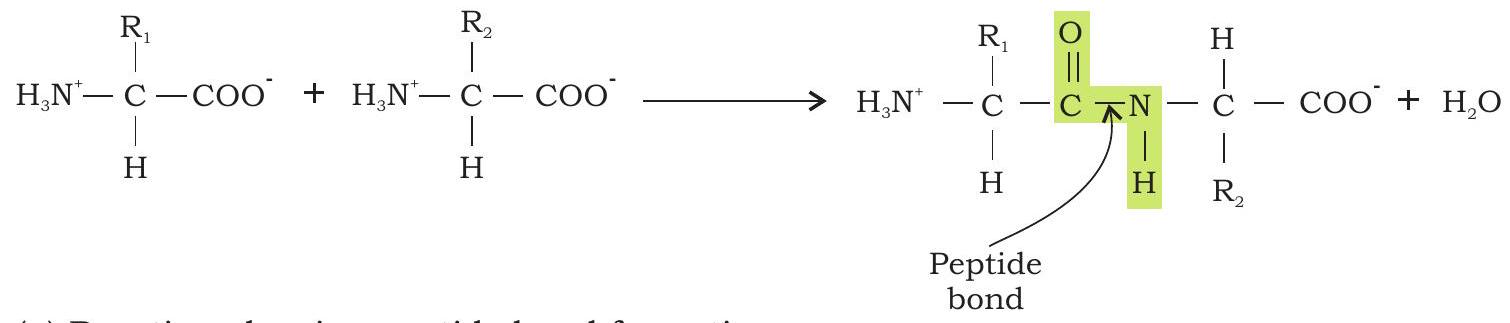
(a) पेप्टाइड बंध निर्माण को दर्शाती अभिक्रिया
प्रोटीन की प्राथमिक संरचना अमीनो अम्लों की श्रृंखला का क्रम है
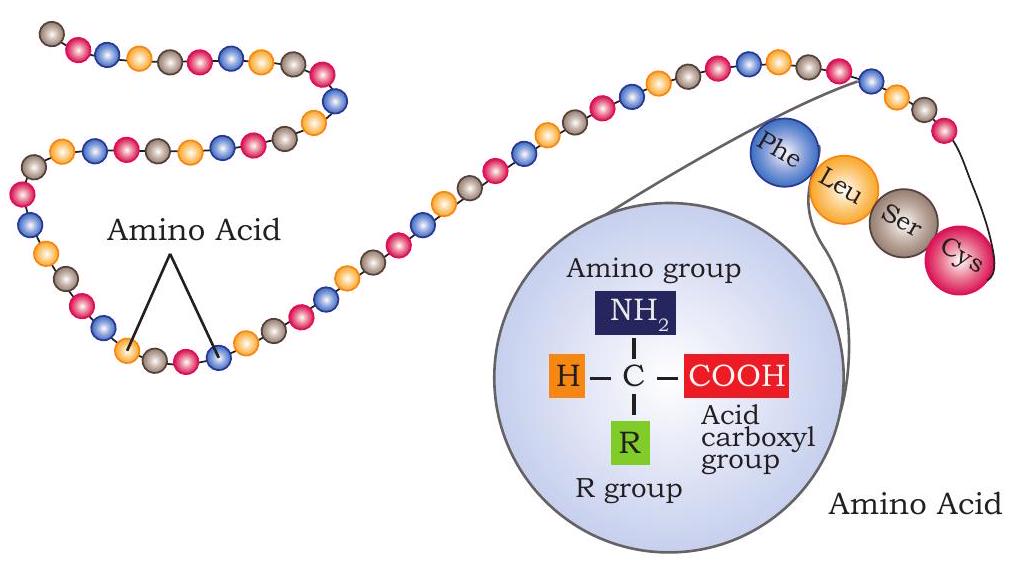
(b) पेप्टाइड बंध से जुड़े अमीनो अम्लों की रैखिक क्रम वाली लंबी पॉलीपेप्टाइड श्रृंखला
चित्र 3.24: प्रोटीन की प्राथमिक संरचना (a) पेप्टाइड बंध निर्माण को दर्शाती अभिक्रिया
(b) लंबी पॉलीपेप्टाइड श्रृंखला जो अमीनो अम्लों की रैखिक श्रृंखला को पेप्टाइड बंध द्वारा जोड़ती है
पेप्टाइड बंध (जिसे एमाइड बंध भी कहा जाता है) एक अमीनो अम्ल के α-कार्बॉक्सिल समूह को दूसरे अमीनो अम्ल के α-अमीनो समूह से जोड़कर बनता है। दो अमीनो अम्लों के बीच पेप्टाइड बंध बनने पर जल अणुओं की हानि होती है। इसलिए, पॉलीपेप्टाइड में प्रत्येक अमीनो अम्ल इकाई को अवशेष कहा जाता है।
इस अभिक्रिया का साम्य जल अपघटन की ओर अधिक होता है न कि संश्लेषण की ओर। इसलिए, पेप्टाइड बंध के जैव-संश्लेषण के लिए मुक्त ऊर्जा की आवश्यकता होती है।
श्रृंखला बनाने वाले अमीनो अम्लों की संख्या के आधार पर, पेप्टाइड्स को डाइपेप्टाइड (दो अमीनो अम्ल इकाइयों वाला), ट्राइपेप्टाइड (तीन अमीनो अम्ल इकाइयों वाला) आदि कहा जा सकता है। एक पॉलीपेप्टाइड श्रृंखला में ध्रुवता होती है क्योंकि इसके दोनों सिरे भिन्न होते हैं। दोनों सिरों को अमीनो (या $\mathrm{N}$-टर्मिनल) और कार्बॉक्सी (या $\mathrm{C}$-टर्मिनल) सिरे कहा जाता है। किसी पॉलीपेप्टाइड का नामकरण करते समय, परंपरा यह है कि $\mathrm{N}$-टर्मिनल अवशेष, जो बाईं ओर होता है, पहले लिखा जाता है और $\mathrm{C}$-टर्मिनल अवशेष अंत में लिखा जाता है। इस प्रकार, पेंटापेप्टाइड Tyr-Ala-Gly-Ser-Leu (YAGSL) में, टायरोसीन अमीनो-टर्मिनल अवशेष है और ल्यूसीन कार्बॉक्सी-टर्मिनल अवशेष है।
एक पॉलीपेप्टाइड घटक में, अमीनो अम्लों का नामकरण उन सभी अमीनो अम्लों में -yl प्रत्यय जोड़कर किया जाता है (क्योंकि ये सभी एसिल समूह हैं) सिवाय अंतिम अमीनो अम्ल के जिसमें कोई प्रत्यय नहीं जोड़ा जाता। उदाहरण के लिए, पेन्टापेप्टाइड Tyr-Ala-Gly-Ser-Leu (YAGSL) का नाम Tyrosyl-L-alanyl-L-glycyl-L-seryl-L-leucine है। यदि इस पेन्टापेप्टाइड में अमीनो अम्लों की अनुक्रमणिका ज्ञात नहीं है, तो संक्षेप (Tyr, Ala, Gly, Ser, Leu) होगा, कोष्ठक और अल्पविराम दर्शाते हैं कि केवल पेन्टापेप्टाइड की संरचना ही ज्ञात है।
औसतन, अधिकांश प्राकृतिक पॉलीपेप्टाइडों में 50 से 2000 अमीनो अम्ल अवशेष होते हैं। एक अमीनो अम्ल अवशेष का औसत आण्विक भार लगभग 110 डाल्टन होता है (डाल्टन द्रव्यमान की इकाई है)।
बॉक्स 2
पेप्टाइड बॉन्ड की संरचना
पेप्टाइड बॉन्ड द्वारा जुड़े दो अमीनो अम्लों के छह परमाणु एक ही समतल में होते हैं, अर्थात् इसकी संरचना समतलीय होती है। ये परमाणु पहले अमीनो अम्ल का α-कार्बन परमाणु और CO समूह, तथा दूसरे अमीनो अम्ल का NH समूह और α-कार्बन होते हैं। समतलीय संरचना अनुनादीय अन्योन्यक्रियाओं का परिणाम है जो पेप्टाइड बॉन्ड को लगभग 40% द्विबंधीय प्रकृति प्रदान करती हैं। इस द्विबंधीय प्रकृति के कारण पेप्टाइड बॉन्ड मुक्त रूप से घूर्णन नहीं कर सकता।
पॉलिपेप्टाइड रीढ़ की लचीलापन
प्रोटीन की रीढ़ कठोर समतलीय पेप्टाइड बॉन्डों की एक जुड़ी हुई श्रृंखला होती है। आंशिक द्विबंधीय प्रकृति वाले पेप्टाइड बॉन्ड के विपरीत, −NH₂ समूह और α-C के बीच का बंध, तथा α-C और −COOH समूह के बीच का बंध शुद्ध एकल बंध होते हैं। पेप्टाइड बॉन्ड के निकटस्थ दो बंधों का घूर्णन विभिन्न दिशाएँ उत्पन्न करता है। प्रत्येक अमीनो अम्ल अवशेष से जुड़े इन दो बंधों के घूर्णन की स्वतंत्रता के कारण प्रोटीन के मुड़ने के कई संभावित तरीके होते हैं। इन बंधों के घूर्णन को कोण द्विआयामी कोणों (टॉर्शन कोणों) द्वारा निर्दिष्ट किया जाता है। Ca-N बंध के परितः घूर्णन कोण को फाई (φ) कहा जाता है। Ca-C बंध के बीच घूर्णन कोण को प्सी (ψ) कहा जाता है। किसी भी बंध के सामने से देखने पर घड़ी की दिशा में घूर्णन धनात्मक मान के अनुरूप होता है। φ और ψ कोण पॉलिपेप्टाइड श्रृंखला का मार्ग निर्धारित करते हैं। परंपरा के अनुसार, दोनों φ और ψ को उस संरचना में 0° माना जाता है जिसमें दो पेप्टाइड बॉन्ड एक ही कार्बन से समतल में जुड़े होते हैं। द्विआयामी कोण φ और ψ के मान −180° से +180° के बीच कोई भी हो सकते हैं, परंतु अधिकांश मान वर्जित होते हैं। वह संरचना जिसमें φ और ψ दोनों 0° हों, भी वर्जित होती है क्योंकि पॉलिपेप्टाइड रीढ़ के परमाणुओं और अमीनो अम्ल साइड श्रृंखलाओं के बीच स्थानिक व्याधिका होती है।
रामचंद्रन आरेख
यदि प्रत्येक अमीनो अम्ल अवशेष के लिए φ और ψ के मान दिए गए हों, तो पूरी तरह फैली हुई पॉलिपेप्टाइड श्रृंखला की संरचना निर्धारित की जा सकती है। 1963 में जी.एन. रामचंद्रन ने पहचाना कि पॉलिपेप्टाइड श्रृंखला में कोई अमीनो अम्ल अवशेष φ और ψ के किसी भी युग्म मान को नहीं ले सकता। परमाणुओं को कठोर/ठोस गोलों के रूप में मानकर φ और ψ के स्वीकार्य मानों की भविष्यवाणी की जा सकती है। φ और ψ के स्वीकार्य मानों को एक द्वि-आयामीय आरेख पर दर्शाया जा सकता है जिसे रामचंद्रन आरेख कहा जाता है। पॉली-L-सेरिन के लिए यह आरेख तीन पृथक् स्वीकार्य क्षेत्र दिखाता है (आकृति में छायांकित)। एक क्षेत्र में वे φ-ψ मान होते हैं जो समानांतर β शीट, प्रतिसमानांतर β शीट और कोलाजन हेलिक्स उत्पन्न करते हैं। दूसरा क्षेत्र दक्षिणावर्त α हेलिक्स उत्पन्न करने वाले φ-ψ मानों को सम्मिलित करता है, और तीसरा क्षेत्र वामावर्त α हेलिक्स रखता है। यद्यपि वामावर्त α हेलिक्स स्थानिक रूप से स्वीकार्य क्षेत्र में आता है, परंतु यह संरचना प्रोटीनों में स्थिरता कम होने के कारण नहीं पाई जाती।
3.4.2 प्रोटीन की द्वितीयक संरचना
प्रोटीन की द्वितीयक संरचना पॉलिपेप्टाइड श्रृंखला की मोड़ से संबंधित है। 1951 में, लाइनस पॉलिंग और रॉबर्ट कोरिय ने दो प्रकार की आवर्ती संरचनाओं का प्रस्ताव रखा जिन्हें α-हेलिक्स और β-प्लीटेड शीट कहा जाता है।
α हेलिक्स
एक समतल पेप्टाइड बॉन्ड वाली पॉलिपेप्टाइड श्रृंखला (\mathrm{C}{\mathrm{a}}-\mathrm{N}) और (\mathrm{C}{\mathrm{a}}-\mathrm{C}) बॉन्ड के चारों ओर मोड़कर एक हेलिकल संरचना बना सकती है जिसे α-हेलिक्स कहा जाता है। इस प्रकार, एक α-हेलिक्स एक छड़ जैसी संरचना होती है (चित्र 3.25)। मुख्य श्रृंखला के NH और CO समूहों के बीच हाइड्रोजन बॉन्ड हेलिक्स को स्थिर करते हैं। प्रत्येक अमीनो अम्ल का CO समूह उस अमीनो अम्ल के NH समूह से हाइड्रोजन बॉन्ड बनाता है जो अनुक्रम में चार अवशेष आगे स्थित होता है। सभी मुख्य श्रृंखला के NH और CO समूह हाइड्रोजन बॉन्ड से जुड़े होते हैं, सिवाय हेलिक्स के अंत के पास स्थित अमीनो अम्लों के। साथ ही, α हेलिक्स लूपों द्वारा जुड़ी होती हैं।
$\alpha$ हेलिक्स दाहिनी दिशा में (घड़ी की सुई की दिशा में) या बाईं दिशा में (घड़ी की सुई के विपरीत दिशा में) हो सकती है। दाहिनी दिशा वाली हेलिक्स स्टेरिक रूप से अधिक स्थिर होती हैं क्योंकि साइड चेन और बैकबोन के बीच टकराव कम होता है। सभी ज्ञात पॉलीपेप्टाइड्स में दाहिनी दिशा वाली $\alpha$ हेलिक्स होती है। प्रोटीनों में हेलिकल सामग्री की उपस्थिति व्यापक रूप से भिन्न होती है। उदाहरण के लिए, फेरिटिन, एक रक्त प्रोटीन जो लोहे के भंडारण में मदद करता है, में इसके अमीनो अम्ल अवशेषों का $75 \%$ हेलिक्स बनाते हैं।

$\hspace{4cm}\alpha$-हेलिक्स लूप्स द्वारा जुड़ी होती हैं
चित्र 3.25: a-हेलिक्स
ये a-हेलिकल संरचनाएं, जो मांसपेशियों के मायोसिन और ट्रोपोमायोसिन तथा बालों के केराटिन में मौजूद हैं, रेशों के कठोर गुच्छों को यांत्रिक मजबूती प्रदान करती हैं।
$\beta$ प्लीटेड शीट
पॉलिंग और कोरी द्वारा सुझाई गई दूसरी प्रकार की आवर्ती संरचना $\beta$ प्लीटेड शीट थी। a-हैलिक्स के विपरीत, $\beta$ प्लीटेड शीट में रैखिक क्रम में दूरस्थ अवशेषों के समूहों के बीच हाइड्रोजन बंध शामिल होते हैं। $\beta$ शीट्स में, प्रोटीन क्रम में व्यापक रूप से अलग-अलग दो या अधिक स्ट्रैंड्स को एक के बाद एक व्यवस्थित किया जाता है, जिनके बीच हाइड्रोजन बंध होते हैं। स्ट्रैंड्स की दिशा के आधार पर, $\beta$ शीट्स दो प्रकार की होती हैं: समानांतर और प्रतिसमानांतर $\beta$ शीट्स (चित्र 3.26)। यदि स्ट्रैंड्स एक ही दिशा में चलते हैं तो उन्हें समानांतर $\beta$ शीट्स कहा जाता है; यदि स्ट्रैंड्स विपरीत दिशा में चलते हैं तो उन्हें प्रतिसमानांतर $\beta$ शीट्स कहा जाता है। समानांतर $\beta$ शीट्स, प्रतिसमानांतर की तुलना में कम मुड़ी होती हैं। शाखित अमीनो अम्ल जैसे वैलिन और आइसोलीयूसिन विस्तारित संरचना रखते हैं, इसलिए वे तंग रूप से लिपटे हुए a हैलिक्स की तुलना में $\beta$ शीट संरचना में अधिक आसानी से फिट हो सकते हैं जहां साइड चेन अधिक भीड़भाड़ वाले होते हैं।

चित्र 3.26: $\beta$ प्लीटेड शीट्स की संरचना
3.4.3 प्रोटीन की तृतीयक संरचना
प्रोटीन में सभी अवशेषों की समग्र त्रि-आयामी व्यवस्था को प्रोटीन की तृतीयक संरचना कहा जाता है। द्वितीयक संरचना के विपरीत, तृतीयक संरचना में अमीनो अम्ल अनुक्रम के व्यापक पहलू शामिल होते हैं। पॉलीपेप्टाइड श्रृंखला में दूरस्थ स्थित अमीनो अम्ल, जो विभिन्न प्रकार की द्वितीयक संरचनाओं में होते हैं, एक-दूसरे से अन्योन्यक्रिया करके प्रोटीन की पूर्णतः मुड़ी हुई संरचना बना सकते हैं। तृतीयक संरचना में डाइसल्फाइड, हाइड्रोजन, हाइड्रोफोबिक और आयनिक जैसी कुछ अतिरिक्त बंधन शामिल होते हैं (चित्र 3.27)। डाइसल्फाइड बंधन सिस्टीन अवशेषों के युग्म के ऑक्सीकरण द्वारा बनते हैं।
ये बंधन प्रोटीन को गोलाकार आकार देते हैं। कुछ एंजाइम, परिवहन प्रोटीन, पेप्टाइड हार्मोन और इम्यूनोग्लोब्यूलिन गोलाकार आकार के होते हैं। तृतीयक संरचना में अमीनो अम्ल अवशेषों के ध्रुवीय $\mathrm{R}$ समूह अपने हाइड्रोफिलिक स्वभाव के कारण बाहरी ओर स्थित होते हैं, और अमीनो अम्ल अवशेषों के अध्रुवीय $\mathrm{R}$ समूह आंतरिक भाग में स्थित होकर हाइड्रोफोबिक अन्योन्यक्रिया बनाते हैं। एक हजार से अधिक प्रोटीनों की त्रि-आयामी संरचना एक्स-रे क्रिस्टलोग्राफी और न्यूक्लियर मैग्नेटिक रेजोनेंस (NMR) तकनीकों द्वारा प्रकट की गई है।
आकृति 3.27: प्रोटीन की तृतीयक संरचना
3.4.4 प्रोटीन की चतुष्कीय संरचना
कुछ प्रोटीन एक से अधिक पॉलीपेप्टाइड उपइकाइयों से बने हो सकते हैं, जो अपनी प्राथमिक संरचना में समान या भिन्न हो सकती हैं। ये उपइकाइयाँ विशिष्ट रूप से एक-दूसरे से जुड़कर एक अपेक्षाकृत बड़ी और जटिल अणु बनाती हैं, अर्थात् चतुष्कीय संरचना। चतुष्कीय संरचना प्रोटीन उपइकाइयों की स्थानिक व्यवस्था होती है। इन उपइकाइयों को हाइड्रोजन बंध, स्थिर वैद्युत अन्योन्यक्रियाएँ, आयनिक बंध और डाइसल्फाइड सेतु द्वारा स्थिर किया जाता है। उपइकाइयों की संख्या के आधार पर चतुष्कीय संरचनाएँ डाइमर, ट्राइमर आदि हो सकती हैं। समान प्रोटीन उपइकाइयाँ होमोडाइमर, होमोट्राइमर आदि बनाती हैं जबकि असमान उपइकाइयाँ हेटेरोडाइमर, हेटेरोट्राइमर आदि बनाती हैं। हीमोग्लोबिन की चतुष्कीय संरचना आकृति 3.28 में दी गई है।
3.5 न्यूक्लिक अम्ल
कोशिका अंगिकाएँ, अर्थात् केन्द्रक, माइटोकॉन्ड्रिया और हरितलवक, इन सभी के भीतर न्यूक्लिक अम्ल उपस्थित होते हैं। केन्द्रक के भीतर न्यूक्लिक अम्ल हिस्टोन प्रोटीनों से जुड़कर क्रोमैटिन बनाते हैं। न्यूक्लिक अम्ल न्यूक्लियोटाइडों के बहुलक होते हैं जो फॉस्फोडाइएस्टर बंधनों द्वारा जुड़े होते हैं। कोशिकाओं में न्यूक्लिक अम्लों के दो प्रकार उपस्थित होते हैं—डीऑक्सीराइबोन्यूक्लिक अम्ल (DNA) और राइबोन्यूक्लिक अम्ल (RNA)। DNA आनुवंशिक पदार्थ के रूप में कार्य करता है और एक पीढ़ी से दूसरी पीढ़ी तक सूचना का वहन करता है। यद्यपि, RNA कुछ विषाणुओं में आनुवंशिक पदार्थ के रूप में कार्य करता है।
DNA और RNA के न्यूक्लियोटाइड नाइट्रोजनीय क्षार, शर्करा और फॉस्फेट से बने होते हैं। न्यूक्लिक अम्लों में उपस्थित शर्करा पेन्टोज शर्करा होती है जो दो प्रकार की होती है; DNA में उपस्थित पेन्टोज 2’-डीऑक्सी-D-राइबोज़ होती है और RNA में उपस्थित पेन्टोज D-राइबोज़ होती है। दोनों पेन्टोज बंद पाँच-सदस्यीय वलय के रूप में उपस्थित होती हैं (चित्र 3.29)। न्यूक्लियोटाइडों की पेन्टोज़ को क्रमांकित करने के लिए कार्बन संख्याओं को प्राइम (’) चिह्न दिया जाता है ताकि इन्हें नाइट्रोजनीय क्षारों की संख्याओं से भिन्न किया जा सके।

चित्र 3.29: न्यूक्लिक अम्लों में उपस्थित पेन्टोज शर्कराओं की संरचना
नाइट्रोजनीय क्षार दो प्रकार के होते हैं; प्यूरीन्स और पिरिमिडिन्स। डीएनए और आरएनए के दो प्यूरीन क्षार एडेनिन (A) और ग्वानिन (G) हैं। पिरिमिडिन्स में, साइटोसिन (C) दोनों डीएनए और आरएनए में मौजूद है, थायमिन (T) केवल डीएनए में मौजूद है और यूरेसिल (U) केवल आरएनए में मौजूद है। पांच प्रमुख क्षारों की संरचना (चित्र 3.30) में दिखाई गई है। प्यूरीन और पिरिमिडिन क्षारों में एरोमेटिक रिंग संरचनाएं होती हैं जो $260 \mathrm{~nm}$ के निकट तरंगदैर्ध्य पर प्रकाश को अवशोषित करती हैं।

चित्र 3.30: न्यूक्लिक अम्लों में मौजूद नाइट्रोजनीय क्षारों की संरचना
एक क्षार (या तो प्यूरीन या पिरिमिडिन), एक पेन्टोज शर्करा इकाई और एक फॉस्फेट समूह को आपस में जोड़कर एक न्यूक्लियोटाइड बनाया जाता है। दूसरी ओर, जब केवल एक क्षार को पेन्टोज शर्करा से जोड़ा जाता है और फॉस्फेट समूह नहीं होता, तो उसे न्यूक्लियोसाइड कहा जाता है। DNA के चार न्यूक्लियोसाइड्स हैं—डिऑक्सीएडेनोसिन, डिऑक्सीग्वानोसिन, डिऑक्सीसिटिडिन और डिऑक्सीथाइमिडिन। DNA में मौजूद न्यूक्लियोटाइड्स को डिऑक्सीराइबोन्यूक्लियोटाइड्स या डिऑक्सीराइबोन्यूक्लियोसाइड-5’-मोनोफॉस्फेट्स कहा जाता है, जो DNA की संरचनात्मक इकाई होते हैं। ये चार प्रकार के होते हैं: डिऑक्सीएडेनिलेट (डिऑक्सीएडेनोसाइन-5’-मोनोफॉस्फेट; dAMP), डिऑक्सीग्वानिलेट (डिऑक्सीग्वानोसाइन-5’-मोनोफॉस्फेट; dGMP), डिऑक्सीसिटिडिलेट (डिऑक्सीसिटिडिन-5’-मोनोफॉस्फेट; dCMP) और डिऑक्सीथाइमिडिलेट (डिऑक्सीथाइमिडिन-5’-मोनोफॉस्फेट; dTMP) (चित्र 3.31)। DNA में मौजूद न्यूक्लियोटाइड्स को ’d’ उपसर्ग से दर्शाया जाता है, क्योंकि ये राइबोज की बजाय डिऑक्सीराइबोज शर्करा रखते हैं।
RNA के चार न्यूक्लियोसाइड्स हैं—एडेनोसिन, ग्वानोसिन, सिटिडिन और यूरिडिन। जब ये किसी फॉस्फेट समूह से जुड़ जाते हैं, तो इन्हें राइबोन्यूक्लियोटाइड्स या राइबोन्यूक्लियोसाइड-5’-मोनोफॉस्फेट कहा जाता है। ये भी चार प्रकार के होते हैं: एडेनिलेट (एडेनोसाइन-5’-मोनोफॉस्फेट; AMP), ग्वानिलेट (ग्वानोसाइन-5’-मोनोफॉस्फेट; GMP), सिटिडिलेट (सिटिडिन-5’-मोनोफॉस्फेट; CMP) और यूरिडिलेट (यूरिडिन-5’-मोनोफॉस्फेट; UMP)।
3.5.1 पॉलिन्यूक्लियोटाइड श्रृंखला
डीएनए और आरएनए दोनों के न्यूक्लियोटाइड सहसंयोजी रूप से जुड़े होते हैं, जिसमें एक न्यूक्लियोटाइड इकाई की चीनी के 3’ हाइड्रॉक्सिल $(-\mathrm{OH})$ समूह को अगले न्यूक्लियोटाइड की चीनी के 5’ कार्बन परमाणु से जुड़े फॉस्फेट के $-\mathrm{OH}$ समूह से एस्टरिफाइड किया जाता है, जिससे एक फॉस्फोडाइएस्टर लिंकेज बनता है (चित्र 3.32)। एक पॉलिपेप्टाइड श्रृंखला की तरह, एक पॉलिन्यूक्लियोटाइड श्रृंखला में एक विशिष्ट ध्रुवता होती है, अर्थात् अलग $5^{\prime}$ और $3^{\prime}$ सिरे। $5^{\prime}$ सिरे पर चीनी के $\mathrm{C}-5$ ’ पर फॉस्फेट समूह होता है जबकि 3’ सिरे पर राइबोज के $\mathrm{C}-3$ ’ पर मुक्त $-\mathrm{OH}$ समूह होता है। पॉलिन्यूक्लियोटाइड श्रृंखला में आधार क्रम $5^{\prime} \rightarrow 3^{\prime}$ दिशा में लिखा जाता है।
1953 में जेम्स वॉटसन और फ्रांसिस क्रिक ने डीएनए की द्विकुंडलित (त्रिविमीय) संरचना प्रस्तावित की (चित्र 3.33 (b))। इसमें डीएनए की दो पॉलीन्यूक्लियोटाइड श्रृंखलाएँ एक ही अक्ष के चारों ओर लिपटी होती हैं और दक्षिणावर्त द्विकुंडल बनाती हैं। दोनों स्ट्रैंड्स विपरीत दिशाओं में होते हैं, अर्थात् उनके 3’ और 5’ फॉस्फोडाइएस्टर बंध विपरीत दिशाओं में चलते हैं। शर्करा और फॉस्फेट द्विकुंडल की रीढ़ बनाते हैं और ध्रुवीय वातावरण के संपर्क में रहते हैं। दोनों स्ट्रैंड्स के नाइट्रोजनस बेस द्विकुंडल के केंद्र के अंदर स्टैक होते हैं और इसे जलविरोधी बनाते हैं। कुंडल के भीतर एक स्ट्रैंड का प्रत्येक न्यूक्लियोटाइड बेस समान तल में दूसरे स्ट्रैंड के बेस के साथ हाइड्रोजन बंध बनाता है। एक स्ट्रैंड का A दूसरे स्ट्रैंड के T के साथ दो हाइड्रोजन बंध बनाता है (A = T) और इसके विपरीत, तथा एक स्ट्रैंड का G दूसरे स्ट्रैंड के C के साथ तीन हाइड्रोजन बंध बनाता है (G ≡ C) और इसके विपरीत (चित्र 3.33 (a))।
डीएनए की वॉटसन-क्रिक संरचना को B-DNA भी कहा जाता है। B-DNA डीएनए का सबसे स्थिर रूप है। अन्य दो संरचनात्मक रूप हैं A-DNA और Z-DNA। A-DNA दक्षिणावर्त द्विकुंडल होता है। यह चौड़ा होता है और प्रति कुंडल 11 बेस जोड़े होते हैं। Z-DNA वामावर्त द्विकुंडल होता है जिसमें प्रति कुंडल 12 बेस जोड़े होते हैं।
डीएनए के दो स्ट्रैंड्स के बीच बेस जोड़ हाइड्रोजन बॉन्ड से बने होते हैं [चित्र 3.33 (a)]। गर्म करने पर बेस जोड़ों के बीच हाइड्रोजन बॉन्ड टूट जाते हैं, जिससे डीएनए के दो स्ट्रैंड्स अलग हो जाते हैं—इसे डिनेचुरेशन या मेल्टिंग कहते हैं। वह तापमान जिस पर आधा डीएनए डिनेचुर हो जाता है, उसे मेल्टिंग तापमान (Tₘ) कहते हैं। गर्मी के अलावा, अम्ल या क्षार भी मेल्टिंग का कारण बन सकते हैं। यदि तापमान को Tₘ से नीचे लाया जाए, तो मेल्टिंग से अलग हुए न्यूक्लिक एसिड के स्ट्रैंड स्वतः फिर से जुड़कर डबल हेलिक्स बना सकते हैं। इस पुनः संगठन या रिनेचुरेशन प्रक्रिया को एनीलिंग कहा जाता है।
3.5.2 आरएनए के प्रकार
मैसेंजर आरएनए (mRNA)
यह एकल स्ट्रैंड वाली रैखिक पॉलीराइबोन्यूक्लिओटाइड श्रृंखला होती है जो डीएनए से राइबोसोम तक जेनेटिक सूचना ले जाती है। इसके 5’ सिरे पर UTR (अनट्रांसलेटेड क्षेत्र) होता है, जिसमें पॉलीपेप्टाइड संश्लेषण के लिए कोई जेनेटिक सूचना नहीं होती। इसके बाद प्रारंभिक कोडन, कोडिंग क्षेत्र और स्टॉप कोडन आते हैं। 3’ सिरे पर एक और UTR मौजूद होता है (चित्र 3.34)। यूकैरियोटिक mRNA के 5’ सिरे पर ग्वानिलेट होता है जिसका N-7 स्थान पर मेथिलेशन होता है—इस प्रक्रिया को कैपिंग कहते हैं। mRNA के 3’ सिरे पर पॉलीएडेनिलेशन (कई एडेनिलेट अवशेषों की जोड़) होती है।
चित्र 3.34: एक विशिष्ट प्रोकैरियोटिक mRNA की आरेखीय प्रस्तुति
राइबोसोमल RNA (rRNA)
यह राइबोसोमों की संरचनात्मक घटक बनाती है। 70S प्रोकैरियोटिक राइबोसोम में छोटे उपइकाई (30S) में 16S rRNA होती है, बड़े उपइकाई (50S) में 23S और 5S rRNAs होती हैं। यूकैरियोटिक राइबोसोम (80S) में छोटे उपइकाई (40S) में 18S rRNA होती है और बड़े उपइकाई (60S) में 28S, 5.8S और 5S rRNAs होती हैं।
ट्रांसफर RNA (tRNA)
ये छोटी RNA अणु होते हैं जो प्रोटीन संश्लेषण के दौरान अमीनो अम्लों को राइबोसोम तक पहुंचाते हैं। यह एकल राइबोपॉलिन्यूक्लियोटाइड श्रृंखला होती है जो चार भुजाओं को बनाने के लिए मुड़ी हुई होती है। स्वीकारकर्ता भुजा में $3^{\prime} \mathrm{OH}$ सिरे पर CCA अनुक्रम होता है जो अमीनो अम्ल बंधन स्थल होता है (चित्र 3.35)। एंटीकोडोन भुजा में एंटीकोडोन होता है, तीन आधारों का एक समूह जो अनुवाद के दौरान mRNA के विशिष्ट कोडॉन को पहचानता है।

चित्र 3.35: tRNA अणु की संरचना
सारांश
कार्बोहाइड्रेट कार्बन, हाइड्रोजन और ऑक्सीजन परमाणुओं से बने होते हैं, और जंतु और पौधों के ऊतकों में व्यापक रूप से वितरित होते हैं।
कार्बोहाइड्रेटों को 4 प्रमुख वर्गों में वर्गीकृत किया जाता है, अर्थात् मोनोसैकेराइड्स (जैसे ग्लूकोज, राइबोज), डाइसैकेराइड्स (जैसे सुक्रोज, लैक्टोज), ओलिगोसैकेराइड्स (जैसे रैफिनोज) और पॉलीसैकेराइड्स (जैसे स्टार्च, ग्लाइकोजन)।
मोनोसैकेराइड्स को ट्राइओस, टेट्रोस, पेंटोस, हेक्सोस आदि के रूप में वर्गीकृत किया जा सकता है, अणु में कार्बन परमाणुओं की संख्या के आधार पर।
पेंटोज शर्करा जैसे कि राइबोज न्यूक्लिक अम्लों, सहएंजाइमों का एक महत्वपूर्ण घटक होता है।
दो मोनोसैकेराइड ग्लाइकोसिडिक बंध द्वारा जुड़कर एक डाइसैकेराइड बनाते हैं (उदाहरण, सुक्रोज)।
पॉलीसैकेराइड ऊर्जा के भंडारण रूप के रूप में और संरचनात्मक घटक के रूप में भी विभिन्न भूमिकाएँ निभाते हैं।
लिपिड जीवित जीवों में पाए जाने वाले कार्बनिक यौगिक होते हैं। ये ग्लिसरॉल से एस्टर बंध द्वारा जुड़े हाइड्रोफोबिक फैटी अम्ल श्रृंखलाओं से बने होते हैं।
फैटी अम्ल लंबी श्रृंखला वाले हाइड्रोकार्बन होते हैं जिनमें कार्बोक्सिलिक अम्ल समूह होता है। फैटी अम्ल संतृप्त (कोई डबल बंध नहीं) या असंतृप्त (एक या अधिक डबल बंध) हो सकते हैं। फैटी अम्लों का नामकरण कुल कार्बनों की संख्या, कुल डबल बंधों की संख्या और डबल बंधों की स्थिति के आधार पर होता है।
लिपिड को व्यापक रूप से दो वर्गों में वर्गीकृत किया जाता है—सरल और यौगिक लिपिड।
सरल लिपिड में ट्राइएसिलग्लिसरॉल और मोम शामिल होते हैं, जो क्रमशः ग्लिसरॉल के साथ फैटी अम्लों के एस्टर और उच्च आणविक भार वाले अल्कोहल के साथ फैटी अम्लों के एस्टर होते हैं।
यौगिक लिपिड में झिल्ली लिपिड शामिल होते हैं जो दो प्रकार के होते हैं, ग्लिसरोफॉस्फोलिपिड और स्फिंगोलिपिड। यौगिक लिपिड उभयदेशी अणु होते हैं जो हाइड्रोफिलिक फॉस्फेट पूंछों से बने होते हैं।
ग्लिसरोफॉस्फोलिपिड में ग्लिसरॉल बैकबोन होता है और स्फिंगोलिपिड में स्फिंगॉइड बेस बैकबोन होता है।
स्टेरॉयड यौगिक लिपिड का एक अन्य वर्ग है जो चार संयुक्त रिंग संरचना से बना होता है। कोलेस्ट्रॉल जानवरों में पाया जाने वाला सबसे सामान्य स्टेरॉयड है। यह सभी स्टेरॉयड हार्मोनों और विटामिन डी का अग्रद्रव्य होता है।
अमीनो अम्ल ऐसे कार्बनिक यौगिक होते हैं जिनमें एमीन $\left(-\mathrm{NH}_{2}\right)$ और कार्बोक्सिल (-COOH) कार्यात्मक समूह होते हैं, साथ ही प्रत्येक अमीनो अम्ल के लिए विशिष्ट एक साइड चेन (R समूह) भी होता है।
20 मानक अमीनो अम्ल होते हैं और कुछ गैर-मानक अमीनो अम्ल (जैसे 4-हाइड्रॉक्सी प्रोलिन, 5-हाइड्रॉक्सी लाइसिन, आदि) और कुछ गैर-प्रोटीन अमीनो अम्ल (जैसे, L-ऑर्निथिन, L-सिट्रुलिन, आदि) भी होते हैं।
एक पॉलिपेप्टाइड श्रृंखला में, अमीनो अम्ल पेप्टाइड बॉन्ड के माध्यम से सहसंयोजक रूप से रैखिक तरीके से जुड़कर एक प्रोटीन बनाते हैं।
प्रोटीन संरचनाओं के चार स्तर होते हैं, अर्थात् प्राथमिक, द्वितीयक, तृतीयक और चतुष्क।
प्रोटीन की प्राथमिक संरचना पेप्टाइड बॉन्ड के माध्यम से जुड़ी हुई अमीनो अम्ल अनुक्रमों की रैखिक श्रृंखला होती है।
प्रोटीन की द्वितीयक संरचना पॉलिपेप्टाइड की त्रिविमीय रूप होती है।
द्वितीयक संरचनाओं के दो प्रमुख प्रकार α-हैलिक्स और $\beta$-शीट्स होते हैं।
तृतीयक संरचना प्रोटीन की त्रिविमीय व्यवस्था होती है।
चतुष्क संरचना मुड़े हुए प्रोटीन उप-इकाइयों की जटिल व्यवस्था होती है, जो हाइड्रोजन बॉन्ड, इलेक्ट्रोस्टेटिक अन्योन्यक्रियाओं आदि के माध्यम से स्थिर होती है।
न्यूक्लिक अम्ल न्यूक्लियोटाइड के बहुलक होते हैं जिनमें नाइट्रोजनीय क्षार (एडेनिन, ग्वानिन, साइटोसिन, थाइमिन और यूरासिल), शर्करा और फॉस्फेट होते हैं।
डीऑक्सीराइबोन्यूक्लिक अम्ल (DNA) और राइबोन्यूक्लिक अम्ल (RNA) न्यूक्लिक अम्ल के दो प्रकार हैं।
DNA लगभग सभी जीवों की आनुवंशिक सामग्री होता है सिवाय कुछ वायरसों के जहाँ RNA आनुवंशिक सामग्री होता है।
डीएनए में डिऑक्सीराइबोज शर्करा और थाइमिन होता है जबकि आरएनए में राइबोज शर्करा होता है और थाइमिन के स्थान पर यूरासिल होता है।
डीएनए में, एडेनिन थाइमिन के साथ 2 हाइड्रोजन बंध बनाता है $(A=T)$ और साइटोसिन ग्वानिन के साथ 3 हाइड्रोजन बंध बनाता है $(\mathrm{C} \equiv \mathrm{G})$।
जे. वॉटसन और एफ. क्रिक (1953) ने डीएनए की त्रि-आयामी द्विकुंडलित संरचना का वर्णन किया।
mRNA, tRNA, rRNA आरएनए के प्रमुख प्रकार हैं।
अभ्यास
1. कार्बोहाइड्रेट्स का वर्गीकरण वर्णन कीजिए।
2. ग्लूकोज के D- और L- रूपों में अंतर कीजिए।
3. दो मोनोसैकेराइड्स ग्लूकोज और फ्रक्टोज से बने डाइसैकेराइड की संरचना बनाइए।
4. स्टार्च और ग्लाइकोजन की आंशिक संरचना बनाइए।
5. कार्बोहाइड्रेट्स की प्रमुख कार्य लिखिए।
6. मोनोसैकेराइड्स में समावयवता का वर्णन कीजिए।
7. स्फिंगोलिपिड्स और ग्लिसरोलिपिड्स में अंतर कीजिए।
8. झिल्ली लिपिड्स उभयवर्ती क्यों कहलाते हैं?
9. संतृप्त और असंतृप्त फैटी एसिड्स में अंतर कीजिए।
10. अमीनो अम्लों की विभिन्न श्रेणियों का वर्णन कीजिए।
11. ज्विटरायन क्या है और यह कैसे विकसित होता है?
12. गैर-मानक और गैर-प्रोटीन अमीनो अम्ल क्या हैं?
13. पेप्टाइड बंध कैसे बनते हैं?
14. Lys-Glu-Lys की संरचना बनाइए।
15. प्रोटीन की विभिन्न द्वितीयक संरचनाओं का वर्णन कीजिए।
16. प्रोटीन की तृतीयक और चतुष्कोणीय संरचना में अंतर कीजिए।
17. न्यूक्लिओसाइड्स और न्यूक्लिओटाइड्स में अंतर कीजिए।
१८. डीएनए की प्राथमिक संरचना की व्याख्या कीजिए।
१९. A-T-C-G पॉलीन्यूक्लियोटाइड की संरचना बनाइए।
२०. डीएनए का वाटसन और क्रिक मॉडल समझाइए।
२१. डीएनए की विभिन्न रूपों का वर्णन कीजिए।
२२. टी-आरएनए का क्लोवर लीफ मॉडल वर्णित कीजिए।
२३. कार्बोहाइड्रेट्स में निम्नलिखित में से कौन-से फंक्शनल ग्रुप पाए जाते हैं?
(क) ऐल्कोहॉल और कार्बोक्सिल ग्रुप
(ख) ऐल्डिहाइड और कीटोन ग्रुप
(ग) हाइड्रॉक्सिल और हाइड्रोजन ग्रुप
(घ) ईथर और एस्टर ग्रुप
२४. निम्नलिखित में से कौन-सा अपचायक (नॉन-रिड्यूसिंग) डाइसैकेराइड है?
(क) माल्टोज
(ख) लैक्टोज
(ग) सुक्रोज
(घ) सेलोबायोज
२५. प्रोटीनों की पुनरावृत्त इकाइयाँ होती हैं
(क) ग्लूकोज इकाइयाँ
(ख) अमीनो अम्ल
(ग) फैटी अम्ल
(घ) न्यूक्लियोटाइड
२६. प्रोटीनों की सबसे सामान्य द्वितीयक संरचना निम्नलिखित में से कौन-सी है?
(क) α-हेलिक्स
(ख) β-प्लेटेड शीट
(ग) (क) और (ख) दोनों
(घ) उपर्युक्त में से कोई नहीं
२७. एक न्यूक्लियोटाइड में होता है
(क) नाइट्रोजनीयस बेस, शर्करा और फॉस्फेट
(ख) शर्करा और फॉस्फेट
(ग) नाइट्रोजनीयस बेस और शर्करा
(घ) उपर्युक्त में से कोई नहीं
२८. डीएनए के डबल हेलिक्स की दो स्ट्रैंडें किस बंध द्वारा जुड़ी होती हैं?
(क) सहसंयोजी बंध
(ख) हाइड्रोजन बंध
(ग) ग्लाइकोसिडिक बंध
(घ) फॉस्फोडाइएस्टर बंध
२९. भंडारण लिपिड का उदाहरण कौन-सा है?
(क) फैटी अम्ल
(ख) ट्रायसिलग्लिसरॉल
(ग) स्फिंगोलिपिड्स
(घ) आइकोसेनॉइड्स
३०. ग्लिसरोलिपिड्स में फैटी अम्ल ग्लिसरॉल से किस बंध द्वारा जुड़े होते हैं?
(क) फॉस्फोडाइएस्टर बंध
(ख) ग्लाइकोसिडिक बंध
(ग) पेप्टाइड बंध
(घ) एस्टर बंध



